الکترولیت باتری چیست؟ الکترولیت در باتری لیتیومی چه میکند؟

الکترولیت یک محیط رساناست که یا از جنس جامد است، یا ژل است و یا مایع. الکترولیت باتری جزئی ضروری از باتری است، یعنی باتری بدون آن نمیتواند برق تولید کند. یک الکترولیت از حرکت یونها در بین آند و کاتد در باتری پشتیبانی میکند.
الکترولیت باتری از چه چیزی ساخته شده است؟
در باتریهای لیتیومی محبوب، الکترولیت ترکیبی از محلول نمک لیتیوم هگزا فلوروفسفات است، اما انواع مختلف باتریها الکترولیتهای متفاوتی دارند. به طور کلی، مواد الکترولیت در باتریها به نمکهای محلول، افزودنیها و حلالها تقسیم میشوند. اما واقعا الکترولیت در باتریهای مختلف از چه جنسی است؟ الکترولیت در یک باتری حالت جامد به شکل یک پلیمر است.
الکترولیت باتری نیکل کادمیوم، از جنس هیدروکسید پتاسیم است که یک الکترولیت قلیایی است.
الکترولیت باتری نیکل متال هیدرید، هیدروکسید پتاسیم یا مادهای مشابه است.

در باتریهای لیتیوم یون، الکترولیت معمولی مایع است و همچنین الکترولیتهای جامد یا کلوئیدی هم وجود دارد که اغلب به آنها سلولهای پلیمری میگویند.
الکترولیت باتریهای آلکالاین که معمولا در زندگی روزمره استفاده میشوند، هیدروکسید پتاسیم است.
الکترولیت باتریهای اسید سرب (سیلد اسید)، اسید سولفوریک رقیق شده است.
الکترولیت در باتری لیتیومی چیست؟
به طور کلی، پنج نوع الکترولیت در باتریهای لیتیومی استفاده میشود: محلولهای آبی، الکترولیتهای حالت جامد، الکترولیتهای پلیمری، مایعات یونی و الکترولیتهای هیبریدی.
با توجه به الکترولیت مورد استفاده، باتریها به انواع باتری لیتیومی نمک مذاب با دمای بالا، باتری لیتیومی الکترولیت آلی، باتری لیتیوم غیرآلی الکترولیتی غیرآبی، باتری لیتیومی الکترولیت جامد و باتری لیتیومی تقسیم میشوند.
نحوه عملکرد الکترولیت در باتری لیتیوم یون
مثل همه باتریها، در باتریهای لیتیومی، الکترولیتها به عنوان یک رسانا عمل میکنند و اجازه میدهند یونها بین کاتد و آند در حین شارژ و دشارژ حرکت کنند. در باتری لیتیوم یون، یون از کاتد به آند حرکت میکند و در حین شارژ مجدد، به سمت عقب برمیگردد.
اجزای باتریهای لیتیومی
به استثنای محافظ بیرونی، یک باتری لیتیومی دارای چهار جزء اصلی است: آند، کاتد، جداکننده و الکترولیت که هر کدام وظایف خود را دارند.
۱. آند: در طول شارژ، لیتیوم یون در آند ذخیره و وقتی باتری به یک دستگاه مصرف برق یا با یک سیم برای استفاده از برق وصل میشود، جریان را برای عبور از مدار خارجی آزاد میکند.
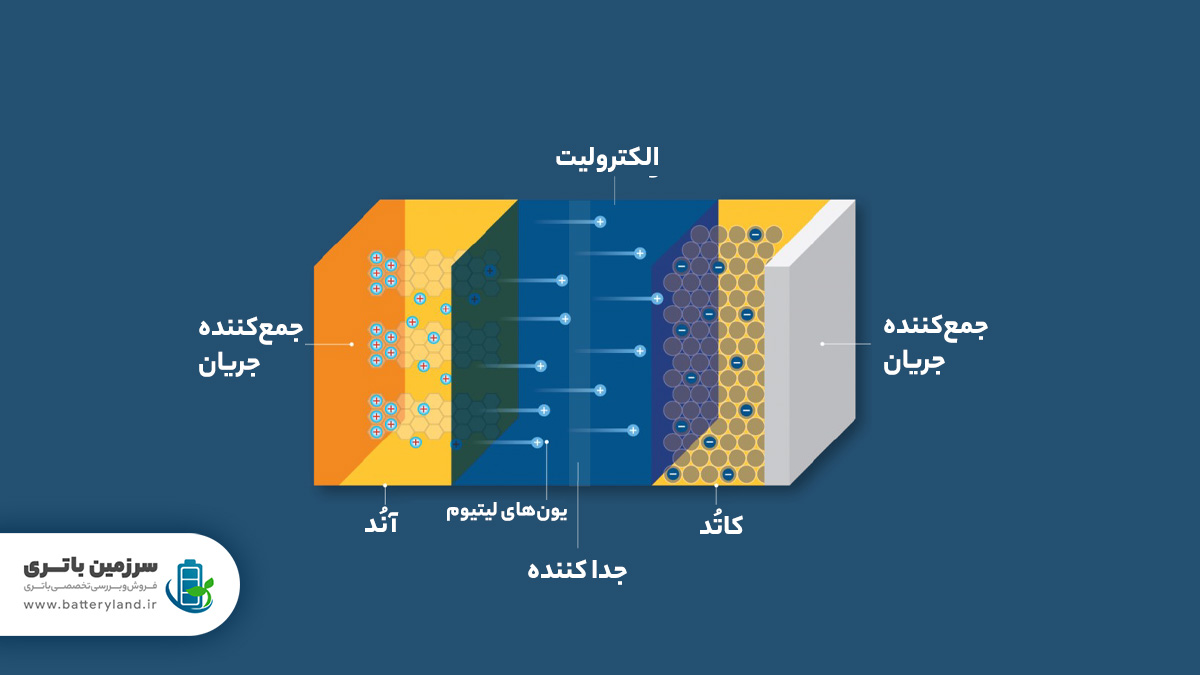
۲. کاتد: ماده کاتدی باتری لیتیوم یونی یک ترکیب لیتیومی و در واقع منبع یونهای لیتیوم است که از یک مدار خارجی الکترون میگیرند و طی یک واکنش الکتروشیمیایی کاهش مییابند.
۳. جداکننده: بین آند و کاتد قرار دارد و مثل یک دیوار ایستاده و از عملکرد باتری محافظت میکند. نقش الکترولیت چیست؟ از جریان الکترون جلوگیری میکند و فقط به جریان یونها اجازه عبور از خلال جداکننده میدهد و به این ترتیب شرایط الکتروشیمیایی باتری را تنظیم میکند.
۴. الکترولیت: الکترولیت بخش مهمی از باتری است که نقش انتقال یونها و هدایت جریان بین کاتد و آند را بر عهده دارد. الکترولیت ترکیبی از نمک، مایعات آلی و مواد افزودنی است و یون را قادر میسازد تا بین الکترودها حرکت کند بدون اینکه الکترون ها جریان پیدا کنند.
باتریهای لیتیومی چگونه کار میکنند؟
وقتی باتری شارژ میشود، یونهای لیتیوم از ترکیب حاوی لیتیوم کاتد استخراج میشوند و از طریق الکترولیت به آند میروند. ماده کربنی آند دارای ساختار لایهای است و ریز منافذ زیادی دارد. یونهای لیتیومی که به آند میرسند در ریز منافذ لایه کربن قرار میگیرند؛ که هرچه مقدارشان بیشتر باشد، ظرفیت شارژ بیشتر است.
وقتی باتری تخلیه میشود (یعنی زمانی که از آن استفاده میکنیم)، یونهای لیتیومِ تعبیه شده در لایه کربن آند خارج شده و به کاتد برمیگردند. هر چه یونهای بیشتری به کاتد برگردند، ظرفیت تخلیه بیشتر میشود. ظرفیت باتری که معمولاً به آن اشاره میکنیم، ظرفیت تخلیه باتری است. در طی فرآیند شارژ و دشارژ باتریهای لیتیوم یونی، یونهای لیتیوم در حالت حرکت از کاتد به آند و به کاتد هستند.
آیا الکترولیت در باتریهای لیتیومی ایمن است؟
بله، الکترولیت موجود در باتری لیتیومی برای استفاده بیخطر است. ممکن است مشکلات آتشسوزی به دلیل گرم شدن بیش از حد حلال الکترولیت در مراحل اولیه باتریهای لیتیومی وجود داشته باشد. با معرفی سیستم مدیریت باتری، این موضوع به درستی مورد توجه قرار گرفته و استفاده از باتریهای لیتیومی نسل جدید بسیار ایمن است. اکنون از الکترولیتهای کلوئیدی استفاده میشود که ایمنتر و احتمال آتش گرفتن آنها کمتر است.
الکترولیتها چگونه بر عملکرد باتری تاثیر میگذارند؟
از آنجایی که الکترولیتها رسانا هستند و به حرکت یونها از کاتد به آند و بازگشتشان به آند کمک میکنند، یک الکترولیت خوب به سرعت جریان حرکت یون را پشتیبانی میکند. برای تسهیل بهتر و کارآمد حرکت یون، الکترولیت باید عنصر فلزی را در هر دو نیمه باتری یا یک نیمه آن داشته باشد که به جذب سریع مولکول یون کمک میکند.

الکترولیت جامد، الکترولیت مایع و الکترولیت ژل
۱. الکترولیت جامد: رسانای جامدی است که به یون اجازه میدهد در یک باتری حالت جامد با ویژگیهای عملکردی الکترولیت مایع یا ژل حرکت کند. الکترولیت حالت جامد خیلی ایمنتر از هر شکل دیگری از الکترولیت است، چون نشتی ندارد. پایداری حرارتی و مکانیکی باتریهای دارای الکترولیت جامد عالی است و با اشتعال پذیری و سرعت تخلیه کم، قابلیت بازیافت خیلی خوب و ویژگیهای ذخیره سازی با چگالی توان پایینی دارند.
۲. الکترولیت مایع: الکترولیت مایع شکلی از الکترولیت است که از حداقل یک نمک و یک ماده افزودنی قطبی غیرآبی مایع تشکیل شده است. حلال میتواند آب و نمک یا اسید میتواند ماده قابل یونیزاسیون باشد. باتریهای سرب اسید از الکترولیتهای مایع استفاده میکنند.
۳. الکترولیت ژل: الکترولیت ژل شبیه یک الکترولیت جامد و الکترولیت مایع است که میتواند مثل یک رسانا عمل کند و حرکت یونها در بین آند و کاتد را فراهم نماید. این الکترولیت ترکیبی از الکترولیتهای مایع و پلیمرهای جامد است.
کم بودن الکترولیت باتری به چه معناست؟ آیا میشود به باتری الکترولیت اضافه کرد؟
وقتی الکترولیت در باتری کم میشود، ظرفیت آن کاهش مییابد و دیگر نمیتواند تا سطح طراحی شده مجددا شارژ شود یا انرژی را برای مدت طولانی تحویل دهد. با این حال، این اتفاق بیشتر در باتریهای سرب اسیدی معمولی رخ میدهد که مهر و موم نشده و در صورت تخلیه الکترولیت باید آب به آن اضافه شود. بنابراین، نیازمند تعمیر و نگهداری منظم است. این مورد درباره باتریهای لیتیوم یونی که کاملاً آب بندی شده و نیازی به تعمیر و نگهداری ندارند صدق نمیکند.
فقط در صورتی میتوانید الکترولیتها را به باتری اضافه کنید که قابل تعمیر باشد؛ یعنی فقط میتوانید الکترولیتها را به یک باتری اسیدی بدون مهر و موم اضافه کنید. به این ترتیب که با باز کردن درب اسید، سطح الکترولیت باتری اسیدی به صورت دستی بررسی میشود و در صورت پایین بودن، برای افزایش سطح الکترولیت باید آب باتری اضافه شود.

نحوه ساخت محلول الکترولیت باتری
میتوانید برای باتریهای اسیدی محلولهای الکترولیت را در خانه با استفاده از اسید سولفوریک و آب درست کنید. بهترین نسبت اختلاط یک قسمت سولفوریک با ۱۰ قسمت آب است تا به درستی رقیق باشد. پس از رقیق شدن، میشود آب اسیدی را به محفظه باتری منتقل کرد.
به منظور ساخت الکترولیت برای باتریهای لیتیومی، باید از عنصری استفاده کرد که برای نصف یا هر دو نیمه باتری بهعنوان الکترولیت استفاده شود؛ همراه با اسید و نمک قدرتمندی که بتواند جریان یونها را در بین کاتدها افزایش دهد.
نتیجهگیری
با توجه به تکنولوژی حاضر، تمام باتریها اعم از لیتیوم، قلیایی، دی اکسید نقره، اسید یا سایر باتریها باید دارای الکترولیت باشند تا حرکت یونها را از کاتد به آند فراهم کند (در باتریهای شارژی به کاتد بروند). الکترولیت باید رسانایی برای حرکت سریع یونها در بین الکترودها باشد تا باتری بتواند به سرعت شارژ شود. جدا از کاتد، آند و جداکننده، الکترولیت جزء جدایی ناپذیر باتری و دارای نقش حساسی است.
منبع: Takoma Battery








































برای نوشتن دیدگاه باید وارد بشوید.